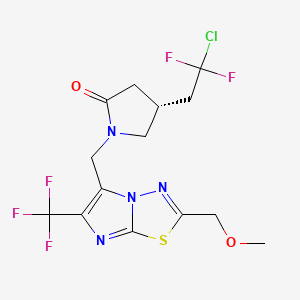
Padsevonil
概要
説明
パドセボニルは、治療抵抗性てんかん患者の未充足ニーズに対応するために開発された、新規抗てんかん薬候補です。 これは、シナプス小胞タンパク質2とγ-アミノ酪酸A受容体の2つの治療標的に作用する、ファーストインクラスの化合物です 。 この二重作用機序により、パドセボニルはシナプス前およびシナプス後の両方に作用し、てんかんの管理に有望な選択肢となります .
準備方法
パドセボニルは、シナプス小胞タンパク質2に対して高い親和性、γ-アミノ酪酸A受容体のベンゾジアゼピン結合部位に対しては低〜中等度の親和性を持つ化合物を設計することを目的とした、医薬品化学プログラムを通じて合成されました 。 パドセボニルの具体的な合成経路と反応条件は、入手可能な文献では明らかにされていません。 この化合物は、合理的設計と薬理プロファイルの最適化を通じて開発されたことが知られています .
化学反応の分析
パドセボニルは、シナプス小胞タンパク質2およびγ-アミノ酪酸A受容体への結合など、さまざまな化学反応を起こします 。 この化合物は、レベチラセタムやブリバラセタムなどの他の抗てんかん薬に比べて結合速度が遅く、シナプス小胞タンパク質2A、2B、および2Cアイソフォームに対して高い親和性を示します 。 パドセボニルは、γ-アミノ酪酸A受容体のベンゾジアゼピン結合部位に対しても低〜中等度の親和性を示し、部分アゴニスト特性を示しています 。 これらの反応から生成される主要な生成物には、パドセボニルと標的タンパク質の結合複合体が含まれます .
科学研究の応用
パドセボニルは、特に薬剤耐性焦点発作のある患者におけるてんかん治療の可能性について、広く研究されてきました 。 臨床試験では、発作頻度を減らし、患者の転帰を改善する有効性が示されています 。 さらに、パドセボニルの独自の作用機序は、てんかんやその他の神経疾患におけるシナプス小胞タンパク質とγ-アミノ酪酸A受容体の役割を研究するための貴重なツールとなっています 。 二重標的プロファイルは、てんかんの管理のための新たな治療戦略の開発に関する知見も提供しています .
科学的研究の応用
Phase IIa Trials
The efficacy of padsevonil has been evaluated in multiple clinical trials, notably the Phase IIa trial which focused on patients with treatment-resistant focal epilepsy. Key findings from this trial include:
- Participants : 55 patients were randomized, with 50 completing the trial.
- Results :
Phase IIb and III Trials
Subsequent trials (EP0091 and EP0092) further assessed this compound's safety and efficacy:
- Design : Randomized, double-blind, placebo-controlled trials involving patients experiencing focal seizures despite treatment with multiple antiepileptic drugs.
- Outcomes : Although primary outcomes did not reach statistical significance in all dose groups, this compound was generally well tolerated with a favorable safety profile .
Safety Profile
This compound has demonstrated a safety profile consistent with earlier studies:
- Adverse Events : Commonly reported treatment-emergent adverse events included somnolence (45.5%), dizziness (43.6%), and headache (25.5%). Importantly, only one patient discontinued due to these events .
- Tolerability : Overall, this compound was well tolerated among participants across various trials, indicating its potential as a viable option for patients with refractory epilepsy .
Comparative Efficacy
To contextualize this compound's efficacy, it is essential to compare it against existing antiepileptic medications:
| Drug | Mechanism of Action | Efficacy in Treatment-Resistant Epilepsy |
|---|---|---|
| This compound | SV2A binding + GABA A receptor modulation | Significant reduction in seizure frequency |
| Levetiracetam | SV2A binding | Moderate efficacy |
| Brivaracetam | SV2A binding | Moderate efficacy |
Case Studies
Several case studies have documented the real-world application of this compound:
- Case Study A : A patient with a history of multiple drug-resistant seizures experienced a significant reduction in seizure frequency after initiating treatment with this compound as an adjunct therapy.
- Case Study B : In another instance, a patient reported improved quality of life and reduced seizure episodes following the introduction of this compound alongside their existing regimen.
These cases underscore the potential benefits of this compound for individuals who have not responded adequately to traditional treatments.
作用機序
類似化合物との比較
パドセボニルは、シナプス小胞タンパク質2とγ-アミノ酪酸A受容体の両方に作用することができる二重標的プロファイルを持つため、抗てんかん薬の中でユニークです 。 類似の化合物には、シナプス小胞タンパク質2Aを選択的なリガンドとする、レベチラセタムやブリバラセタムなどがあります 。 パドセボニルは、3つのシナプス小胞タンパク質2アイソフォームすべてに結合する能力と、γ-アミノ酪酸A受容体のベンゾジアゼピン部位における部分アゴニスト特性を持つため、これらの他の薬剤とは異なります 。 この独自の作用機序により、パドセボニルは、シナプス小胞タンパク質2Aとベンゾジアゼピン部位を標的とする化合物の組み合わせよりも、抗てんかん特性が強化されています .
生物活性
Padsevonil, also known as UCB-0942, is a novel antiepileptic drug candidate developed by UCB Pharma. It represents a first-in-class compound targeting both synaptic vesicle protein 2A (SV2A) and GABA receptors. This dual mechanism of action is designed to enhance antiseizure efficacy while minimizing the side effects commonly associated with traditional antiepileptic drugs.
Target Interactions:
- Synaptic Vesicle Protein 2A (SV2A): this compound binds with high affinity to SV2A, which is crucial for neurotransmitter release. This interaction is believed to correlate with its antiseizure potency.
- GABA Receptors: It also interacts with GABA receptors at the benzodiazepine site, where it acts as a partial agonist. This provides therapeutic effects without inducing significant sedation or tolerance, which are common issues with full agonists.
Clinical Trials and Efficacy
This compound has undergone several clinical trials, notably a randomized Phase IIa trial focusing on treatment-resistant focal epilepsy. The key findings from this trial are summarized below:
| Parameter | This compound Group (n=24) | Placebo Group (n=26) | P-value |
|---|---|---|---|
| ≥75% Seizure Frequency Reduction | 30.8% | 11.1% | 0.067 |
| Median Weekly Seizure Frequency Reduction | 55.2% | 12.5% | 0.026 |
| Treatment-Emergent Adverse Events | 90.9% reported | 63.0% reported | - |
| Common Adverse Events | Somnolence (45.5%), Dizziness (43.6%), Headache (25.5%) | - | - |
The trial included adults experiencing at least four focal seizures per week and who had failed to respond to multiple antiepileptic drugs. After a three-week inpatient period, the results indicated a statistically significant reduction in seizure frequency among those treated with this compound compared to placebo, highlighting its potential efficacy in a challenging patient population .
Safety Profile
This compound demonstrated a favorable safety profile during the trials:
- The most common treatment-emergent adverse events included somnolence, dizziness, and headache.
- Notably, only one patient discontinued treatment due to adverse events, suggesting that this compound may be better tolerated than many existing therapies.
Translational Research Insights
Two PET imaging studies conducted in healthy volunteers helped identify optimal target occupancy levels for this compound:
Q & A
Basic Research Questions
Q. What distinguishes Padsevonil's mechanism of action from other SV2A-targeting antiepileptic drugs (AEDs) like levetiracetam?
this compound uniquely binds to all three synaptic vesicle 2 (SV2) isoforms (SV2A, SV2B, SV2C) with high affinity (pKi: SV2A = 8.5, SV2B = 7.9, SV2C = 8.5), unlike levetiracetam and brivaracetam, which selectively target SV2A. Its dissociation kinetics from SV2A are markedly slower (t1/2 >30 minutes vs. <0.5 minutes for levetiracetam/brivaracetam), suggesting prolonged target engagement. Additionally, this compound acts as a low-affinity partial agonist (40% efficacy vs. zolpidem) at GABAA receptors, combining presynaptic (SV2) and postsynaptic (GABAergic) modulation .
Q. Which preclinical models are most relevant for evaluating this compound's efficacy in drug-resistant epilepsy?
this compound demonstrated robust efficacy in the 6 Hz focal seizure model (mice) and amygdala kindling model (rodents), which predict activity against focal to bilateral tonic-clonic seizures. It also showed dose-dependent protection in chronic models like intrahippocampal kainate (mesial temporal lobe epilepsy) and Genetic Absence Epilepsy Rats from Strasbourg (GAERS). These models are prioritized due to their translational relevance to drug-resistant epilepsy .
Q. How does this compound's dual-target profile influence its therapeutic index in preclinical studies?
In rodent models, this compound exhibited a high therapeutic index, with SV2A occupancy at low doses (ED50 = 0.2 mg/kg) and GABAA receptor engagement at higher doses (ED50 = 36 mg/kg). This separation likely contributes to its favorable safety profile, avoiding excessive GABAergic side effects (e.g., sedation) at therapeutic doses .
Advanced Research Questions
Q. What methodological challenges arise when quantifying this compound's target engagement in vivo?
PET studies using SV2A radioligands (e.g., [11C]UCB-J) must account for this compound’s slow dissociation kinetics. The "Single-step" solution for occupancy calculations may underestimate binding compared to the "Numerical" method, particularly for rapid-acting drugs. Future studies should validate these models for this compound’s unique pharmacokinetic profile .
Q. How can researchers reconcile discrepancies between this compound's preclinical efficacy and mixed clinical trial outcomes?
While this compound showed superior efficacy in preclinical models (e.g., 6 Hz and amygdala kindling), phase IIb trials failed to meet primary endpoints. Potential factors include:
- Patient heterogeneity : Enrolled populations with diverse resistance mechanisms.
- Dosing limitations : Clinical doses may not achieve sufficient SV2B/C or GABAA receptor occupancy.
- Trial design : Overly optimistic endpoints (e.g., ≥75% seizure reduction) vs. preclinical benchmarks .
Q. Does this compound's multi-target action provide synergistic benefits compared to combining SV2A ligands and benzodiazepines?
In the 6 Hz model, this compound outperformed combinations of diazepam + levetiracetam/brivaracetam, suggesting its dual SV2 isoform engagement and partial GABAA agonism confer unique synergies. This contrasts with full GABAA agonists, which risk tolerance and receptor desensitization .
Q. What experimental strategies are critical for optimizing this compound's pharmacokinetic/pharmacodynamic (PK/PD) modeling?
- Microsampling techniques : Dried blood spots (DBS) or volumetric absorptive microsampling (VAMS) enable frequent sampling without compromising animal welfare.
- Cerebrospinal fluid (CSF) analysis : Directly correlates with brain exposure.
- Allometric scaling : Accounts for interspecies differences in metabolic clearance .
Q. Key Methodological Recommendations
- Binding Assays : Use recombinant SV2 isoforms and temperature-controlled (37°C) radioligand displacement to capture this compound’s slow kinetics .
- In Vivo Models : Prioritize chronic epilepsy models (e.g., intrahippocampal kainate) over acute seizure tests (e.g., pentylenetetrazol) to reflect drug-resistant mechanisms .
- Clinical Translation : Incorporate patient-centric sampling and PK/PD modeling to bridge preclinical and clinical dosing .
特性
IUPAC Name |
(4R)-4-(2-chloro-2,2-difluoroethyl)-1-[[2-(methoxymethyl)-6-(trifluoromethyl)imidazo[2,1-b][1,3,4]thiadiazol-5-yl]methyl]pyrrolidin-2-one | |
|---|---|---|
| Source | PubChem | |
| URL | https://pubchem.ncbi.nlm.nih.gov | |
| Description | Data deposited in or computed by PubChem | |
InChI |
InChI=1S/C14H14ClF5N4O2S/c1-26-6-9-22-24-8(11(14(18,19)20)21-12(24)27-9)5-23-4-7(2-10(23)25)3-13(15,16)17/h7H,2-6H2,1H3/t7-/m1/s1 | |
| Source | PubChem | |
| URL | https://pubchem.ncbi.nlm.nih.gov | |
| Description | Data deposited in or computed by PubChem | |
InChI Key |
DCXFIOLWWRXEQH-SSDOTTSWSA-N | |
| Source | PubChem | |
| URL | https://pubchem.ncbi.nlm.nih.gov | |
| Description | Data deposited in or computed by PubChem | |
Canonical SMILES |
COCC1=NN2C(=C(N=C2S1)C(F)(F)F)CN3CC(CC3=O)CC(F)(F)Cl | |
| Source | PubChem | |
| URL | https://pubchem.ncbi.nlm.nih.gov | |
| Description | Data deposited in or computed by PubChem | |
Isomeric SMILES |
COCC1=NN2C(=C(N=C2S1)C(F)(F)F)CN3C[C@H](CC3=O)CC(F)(F)Cl | |
| Source | PubChem | |
| URL | https://pubchem.ncbi.nlm.nih.gov | |
| Description | Data deposited in or computed by PubChem | |
Molecular Formula |
C14H14ClF5N4O2S | |
| Source | PubChem | |
| URL | https://pubchem.ncbi.nlm.nih.gov | |
| Description | Data deposited in or computed by PubChem | |
Molecular Weight |
432.8 g/mol | |
| Source | PubChem | |
| URL | https://pubchem.ncbi.nlm.nih.gov | |
| Description | Data deposited in or computed by PubChem | |
CAS No. |
1294000-61-5 | |
| Record name | Padsevonil [USAN:INN] | |
| Source | ChemIDplus | |
| URL | https://pubchem.ncbi.nlm.nih.gov/substance/?source=chemidplus&sourceid=1294000615 | |
| Description | ChemIDplus is a free, web search system that provides access to the structure and nomenclature authority files used for the identification of chemical substances cited in National Library of Medicine (NLM) databases, including the TOXNET system. | |
| Record name | Padsevonil | |
| Source | DrugBank | |
| URL | https://www.drugbank.ca/drugs/DB14977 | |
| Description | The DrugBank database is a unique bioinformatics and cheminformatics resource that combines detailed drug (i.e. chemical, pharmacological and pharmaceutical) data with comprehensive drug target (i.e. sequence, structure, and pathway) information. | |
| Explanation | Creative Common's Attribution-NonCommercial 4.0 International License (http://creativecommons.org/licenses/by-nc/4.0/legalcode) | |
| Record name | PADSEVONIL | |
| Source | FDA Global Substance Registration System (GSRS) | |
| URL | https://gsrs.ncats.nih.gov/ginas/app/beta/substances/0R1HN52K0N | |
| Description | The FDA Global Substance Registration System (GSRS) enables the efficient and accurate exchange of information on what substances are in regulated products. Instead of relying on names, which vary across regulatory domains, countries, and regions, the GSRS knowledge base makes it possible for substances to be defined by standardized, scientific descriptions. | |
| Explanation | Unless otherwise noted, the contents of the FDA website (www.fda.gov), both text and graphics, are not copyrighted. They are in the public domain and may be republished, reprinted and otherwise used freely by anyone without the need to obtain permission from FDA. Credit to the U.S. Food and Drug Administration as the source is appreciated but not required. | |
Synthesis routes and methods
Procedure details











試験管内研究製品の免責事項と情報
BenchChemで提示されるすべての記事および製品情報は、情報提供を目的としています。BenchChemで購入可能な製品は、生体外研究のために特別に設計されています。生体外研究は、ラテン語の "in glass" に由来し、生物体の外で行われる実験を指します。これらの製品は医薬品または薬として分類されておらず、FDAから任何の医療状態、病気、または疾患の予防、治療、または治癒のために承認されていません。これらの製品を人間または動物に体内に導入する形態は、法律により厳格に禁止されています。これらのガイドラインに従うことは、研究と実験において法的および倫理的な基準の遵守を確実にするために重要です。